Dove nasce, dove si testa, dove si vende: la nuova geografia del farmaco e il ruolo dell’Europa
Negli ultimi due decenni la geografia dell’industria farmaceutica si è trasformata profondamente. Se gli Stati Uniti continuano a rappresentare il principale epicentro globale dell’innovazione biomedica, una parte crescente dello sviluppo scientifico e industriale si sta progressivamente spostando verso l’Asia. La Cina, in particolare, è diventata in pochi anni uno degli attori più dinamici nello sviluppo di nuove molecole e nella conduzione di studi clinici (Drain et al., in PLoS One, 2018). Allo stesso tempo, la produzione farmaceutica è da tempo largamente decentrata verso paesi con costi del lavoro più bassi, soprattutto per la produzione dei principi attivi e per diverse fasi della manifattura (Busfield, in Social Science and Medicine, 2020).
Questo spostamento non è il risultato di un singolo fattore, ma dell’interazione tra tre dinamiche strutturali: la globalizzazione delle catene del valore, la crescente finanziarizzazione del settore farmaceutico e la competizione internazionale per attrarre investimenti in ricerca e sviluppo (Busfield, in Social Science and Medicine, 2020). In questo nuovo scenario, l’Europa rischia progressivamente di trovarsi in una posizione paradossale: grande mercato di consumo e sofisticato regolatore, ma sempre meno centrale nella produzione di innovazione.
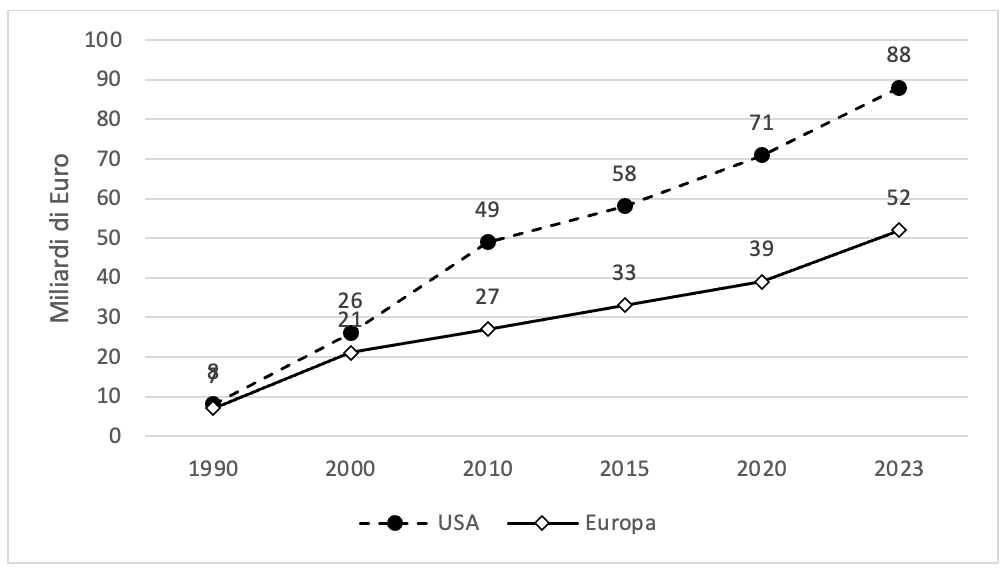
I dati della European Federation of Pharmaceutical Industries and Associations (EFPIA, The Pharmaceutical Industry in Figures, 2025) mostrano con chiarezza questa tendenza. All’inizio degli anni Duemila l’Europa rappresentava circa il 40% degli investimenti globali in ricerca e sviluppo farmaceutica. Oggi la quota europea si è ridotta a poco più del 20%, mentre gli Stati Uniti concentrano oltre la metà della spesa mondiale in R&D del settore (Figura 1).
Figura 1: Investimenti in R&D farmaceutica in Europa e USA 1990-2023.
Fonte: Elaborazione su dati EFPIA 2025.
Nel frattempo, paesi asiatici – con la Cina in posizione dominante – stanno aumentando rapidamente la propria capacità di attrarre investimenti scientifici e industriali (IQVIA Institute, Global Trends in R&D, 2025).
Parallelamente, la geografia della sperimentazione clinica sta cambiando. Sempre più studi clinici vengono condotti in Asia, dove la disponibilità di grandi popolazioni di pazienti, la presenza di grandi centri ospedalieri e un sistema regolatorio sempre più efficiente facilitano il reclutamento e la conduzione dei trial (Figura 2). Questo fenomeno è particolarmente evidente in oncologia e nelle terapie innovative.
Figura 2: Numero di trial per regione 1999-2024.
Fonte: Elaborazione su dati del WHO Global Observatory on Health R&D, 2025
La conseguenza è che una quota crescente delle evidenze cliniche alla base dell’autorizzazione dei nuovi farmaci viene oggi prodotta su popolazioni asiatiche. Questo pone una questione scientifica e regolatoria non banale: quanto sono generalizzabili questi risultati alle popolazioni europee?
In linea di principio, la farmacologia moderna dispone di strumenti metodologici sofisticati per valutare la trasferibilità dei risultati tra popolazioni diverse. Tuttavia, fattori genetici, epidemiologici e ambientali possono influenzare la risposta ai farmaci (Levy, Journal of Comparative Effectiveness Research, 2024). La crescente concentrazione geografica della sperimentazione clinica potrebbe quindi riaprire un dibattito che si credeva superato: quello sulla rappresentatività delle popolazioni negli studi clinici globali.
Ma la questione non è solo scientifica. È anche profondamente economica e politica.
Mentre la ricerca si globalizza e la produzione si delocalizza, l’Europa mantiene uno dei sistemi di accesso al mercato più regolamentati al mondo. Dopo l’autorizzazione centralizzata dell’Agenzia Europea dei Medicinali (EMA), i farmaci devono affrontare complessi processi nazionali di valutazione e negoziazione dei prezzi. Negli ultimi anni questi processi sono diventati sempre più stringenti, soprattutto per le terapie innovative ad alto costo. Strumenti di Health Technology Assessment (HTA), negoziazioni basate sul valore terapeutico e accordi di rimborso condizionato sono ormai parte integrante delle politiche di contenimento della spesa (Vogler, in WHO Publications, 2022).
Dal punto di vista dei sistemi sanitari pubblici, questa evoluzione è comprensibile. I farmaci innovativi – in particolare quelli sviluppati attraverso biotecnologie avanzate o terapie cellulari e geniche – possono avere prezzi molto elevati e mettere sotto pressione i bilanci pubblici. Tuttavia, dal punto di vista industriale, il messaggio che il mercato europeo invia alle imprese è più ambiguo: innovare è possibile, ma monetizzare l’innovazione è sempre più difficile.
Questa trasformazione emerge chiaramente se si osserva la nuova geografia globale dell’industria farmaceutica (Figura 3). Mentre la capacità di generare innovazione resta fortemente concentrata negli Stati Uniti, una quota crescente della sperimentazione clinica come si è già detto si sta spostando verso l’Asia, mentre l’Europa continua a rappresentare uno dei principali mercati regolati per l’accesso ai nuovi farmaci, e lo scarto rispetto all’Asia diventa sempre più piccolo.
Figura 3. Distribuzione geografica globale di innovazione, sperimentazione clinica e mercato farmaceutico, 2024.
Fonte: Elaborazione su dati IQVIA Institute, 2025.
In un settore caratterizzato da elevati costi di ricerca, tempi lunghi di sviluppo e forte incertezza, le imprese allocano naturalmente gli investimenti dove le prospettive di ritorno economico sono più favorevoli. Se la sperimentazione clinica può essere condotta più rapidamente altrove e se il mercato più remunerativo resta quello statunitense, è inevitabile che una parte crescente delle attività di ricerca si concentri fuori dall’Europa (Lou et al.,in medRxiv, 2026; Thiers et al., in Nature Reviews Drug Discovery, 2008).
Il rischio è che il continente si trasformi progressivamente in un “late adopter” dell’innovazione farmaceutica: un mercato importante ma non decisivo, dove i nuovi farmaci arrivano più tardi e dopo aver già generato valore in altri sistemi sanitari.
Questo scenario solleva interrogativi che vanno ben oltre il settore farmaceutico. La questione riguarda infatti il ruolo dell’Europa nella nuova economia globale della conoscenza (Csomòs, 2018). Può un continente che aspira a essere leader nella ricerca scientifica rinunciare a una posizione centrale nello sviluppo industriale dell’innovazione biomedica?
La risposta non può essere semplicemente un allentamento delle politiche di regolazione dei prezzi. La sostenibilità dei sistemi sanitari resta un obiettivo legittimo e imprescindibile. Tuttavia, è necessario interrogarsi su come conciliare tre obiettivi che spesso appaiono confliggenti: promuovere l’innovazione, garantire l’accesso equo ai farmaci e mantenere la sostenibilità finanziaria dei sistemi sanitari.
L’Europa possiede ancora straordinarie risorse scientifiche: università di eccellenza, una solida tradizione di ricerca biomedica e alcuni dei più importanti gruppi farmaceutici globali. Ma queste risorse devono essere sostenute da politiche industriali e scientifiche capaci di attrarre investimenti e di mantenere il continente competitivo nella nuova geografia dell’innovazione. In questa prospettiva, alcuni esperti hanno proposto di ripensare il ruolo dell’Europa non solo come regolatore e acquirente di innovazione sviluppata altrove, ma anche come attore diretto nella produzione di conoscenza. In particolare, Massimo Florio, nell’ambito del Forum Disuguaglianze e Diversità, ha recentemente suggerito che il continente dovrebbe ridurre la dipendenza dalle rendite brevettuali generate in altri contesti, rafforzando invece la ricerca pubblica attraverso infrastrutture comuni su scala europea, sul modello del CERN. Pur trattandosi di una proposta ancora oggetto di dibattito, essa evidenzia la necessità di una strategia più autonoma e proattiva nella politica dell’innovazione farmaceutica.
Negli anni a venire, se una parte crescente della ricerca clinica verrà condotta in Asia, anche la composizione demografica dei trial tenderà inevitabilmente a riflettere le caratteristiche delle popolazioni locali. Questo non implica necessariamente una minore validità scientifica delle evidenze prodotte, ma, come accennato, potrebbe rendere più complessa la valutazione della trasferibilità dei risultati a contesti epidemiologici e genetici differenti, come quelli europei.
Per le autorità regolatorie e per gli organismi di HTA, ciò potrebbe tradursi in una crescente attenzione alla validità esterna degli studi clinici e alla loro capacità di rappresentare la diversità delle popolazioni che utilizzeranno i nuovi trattamenti. Nell’ambito di un sistema sanitario pubblico, assetto che accomuna la gran parte dei paesi europei, le decisioni di rimborso sono sempre più legate alla dimostrazione del valore terapeutico e dell’impatto sulla salute della popolazione (Vogler, in WHO Publications, 2022). Dunque, la qualità e la trasferibilità delle evidenze cliniche diventeranno un elemento sempre più centrale.
In questo senso, la geografia della ricerca clinica non è soltanto una questione industriale o scientifica. È anche una questione di sovranità conoscitiva. Partecipare attivamente alla produzione delle evidenze cliniche significa contribuire a definire le conoscenze su cui si basano le decisioni terapeutiche, regolatorie e di politica sanitaria (Drain et al., in PLoS One, 2018).
Se l’Europa vuole continuare a svolgere un ruolo centrale nella medicina del futuro, dovrà quindi interrogarsi non solo su come finanziare l’innovazione, ma anche su come rimanere uno dei luoghi in cui quell’innovazione viene studiata, sperimentata e validata.